Publikasi baru
Protein yang bertanggung jawab atas penyakit inflamasi genetik teridentifikasi
Terakhir ditinjau: 02.07.2025

Semua konten iLive ditinjau secara medis atau diperiksa fakta untuk memastikan akurasi faktual sebanyak mungkin.
Kami memiliki panduan sumber yang ketat dan hanya menautkan ke situs media terkemuka, lembaga penelitian akademik, dan, jika mungkin, studi yang ditinjau secara medis oleh rekan sejawat. Perhatikan bahwa angka dalam tanda kurung ([1], [2], dll.) Adalah tautan yang dapat diklik untuk studi ini.
Jika Anda merasa salah satu konten kami tidak akurat, ketinggalan zaman, atau dipertanyakan, pilih dan tekan Ctrl + Enter.
Sebuah tim peneliti yang dipimpin oleh Dr. Hirotsugu Oda dari CECAD Cluster of Excellence for Aging Research di University of Cologne telah menemukan peran yang dimainkan oleh kompleks protein tertentu dalam beberapa bentuk disregulasi imun. Hasil ini dapat mengarah pada pengembangan pendekatan terapeutik baru yang bertujuan untuk mengurangi autoinflasi dan "memulihkan" sistem imun pasien yang menderita disfungsi genetik kompleks protein ini.
Penelitian yang berjudul, "Biallelic human SHARPIN loss of function induces autoinflammation and immunodeficiency," diterbitkan dalam jurnal Nature Immunology.
Kompleks perakitan ubikuitin linier (LUBAC), yang terdiri dari protein HOIP, HOIL-1, dan SHARPIN, telah lama dikenal karena perannya yang penting dalam menjaga homeostasis imun. Penelitian sebelumnya pada tikus telah menunjukkan konsekuensi parah dari hilangnya SHARPIN, yang menyebabkan dermatitis parah akibat kematian sel kulit yang berlebihan. Namun, konsekuensi kesehatan spesifik dari defisiensi SHARPIN pada manusia masih belum jelas.
Tim peneliti melaporkan untuk pertama kalinya dua orang dengan defisiensi SHARPIN yang menunjukkan gejala autoinflasi dan defisiensi imun, tetapi secara tak terduga tidak menunjukkan masalah dermatologis seperti yang terjadi pada tikus.
Setelah penyelidikan lebih lanjut, individu-individu ini ditemukan memiliki respons NF-κB kanonik yang terganggu, suatu jalur respons imun yang penting. Mereka juga memiliki peningkatan kerentanan terhadap kematian sel yang disebabkan oleh anggota superfamili faktor nekrosis tumor (TNF). Pengobatan satu pasien yang kekurangan SHARPIN dengan terapi anti-TNF, yang secara khusus menghambat kematian sel yang disebabkan TNF, menghasilkan resolusi autoinflasi yang lengkap pada tingkat sel dan dalam presentasi klinis.
Studi ini menunjukkan bahwa kematian sel yang berlebihan dan tidak terkendali memainkan peran penting dalam penyakit radang genetik manusia. Tim Oda menambahkan defisiensi SHARPIN sebagai anggota baru dari sekelompok penyakit radang genetik manusia yang mereka usulkan untuk disebut "kesalahan bawaan kematian sel."
Perlindungan terhadap disregulasi imun Penelitian ini dimulai di laboratorium Dr. Dan Kastner di National Institutes of Health (NIH) di Amerika Serikat. Para ilmuwan di sana berkesempatan untuk mengamati satu pasien yang mengalami episode demam, artritis, radang usus besar, dan defisiensi imun yang tidak dapat dijelaskan sejak kecil.
Setelah memperoleh persetujuan yang diinformasikan, mereka melakukan pengurutan eksom pada pasien dan anggota keluarganya dan menemukan bahwa pasien memiliki varian genetik yang merusak pada gen SHARPIN yang menyebabkan kadar protein SHARPIN tidak terdeteksi. Mereka juga menemukan bahwa sel-sel pasien menunjukkan peningkatan kecenderungan untuk mati baik pada sel yang dikultur maupun pada biopsi pasien.
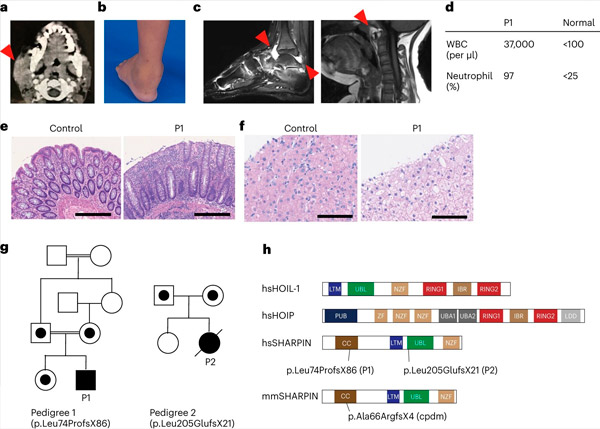
Defisiensi SHARPIN pada manusia menyebabkan autoinflamasi dan glikogenosis hati. Sumber: Nature Immunology (2024). DOI: 10.1038/s41590-024-01817-w
Tim tersebut juga menemukan bahwa perkembangan pusat germinal limfoid – struktur mikro khusus dalam kelenjar adenoid yang penting untuk pematangan sel B sistem imun kita dan, oleh karena itu, untuk produksi antibodi – berkurang secara signifikan karena meningkatnya kematian sel B. Temuan ini menjelaskan defisiensi imun pasien dan menyoroti peran penting LUBAC dalam menjaga homeostasis imun pada manusia.
"Studi kami menyoroti pentingnya LUBAC dalam melindungi terhadap disregulasi imun. Dengan menjelaskan mekanisme molekuler yang mendasari defisiensi LUBAC, kami membuka jalan bagi strategi terapi baru yang bertujuan memulihkan homeostasis imun," kata Oda, penulis utama studi tersebut.
Ia menambahkan: "Salah satu pasien dengan defisiensi SHARPIN telah menggunakan kursi roda selama bertahun-tahun sebelum kami pertama kali melihatnya. Pergelangan kakinya meradang dan sangat sakit untuk berjalan. Diagnosis genetik memungkinkan kami untuk menargetkan jalur molekuler yang tepat yang mendasari kondisinya."
Sejak pasien mulai menerima terapi anti-TNF, ia telah bebas dari gejala selama hampir tujuh tahun. "Sebagai seorang dokter dan ilmuwan, saya senang memiliki kesempatan untuk memberi dampak positif pada kehidupan satu pasien melalui penelitian kami," Oda menyimpulkan.
