Mempelajari mekanisme ruam kulit akibat obat
Terakhir ditinjau: 14.06.2024

Semua konten iLive ditinjau secara medis atau diperiksa fakta untuk memastikan akurasi faktual sebanyak mungkin.
Kami memiliki panduan sumber yang ketat dan hanya menautkan ke situs media terkemuka, lembaga penelitian akademik, dan, jika mungkin, studi yang ditinjau secara medis oleh rekan sejawat. Perhatikan bahwa angka dalam tanda kurung ([1], [2], dll.) Adalah tautan yang dapat diklik untuk studi ini.
Jika Anda merasa salah satu konten kami tidak akurat, ketinggalan zaman, atau dipertanyakan, pilih dan tekan Ctrl + Enter.
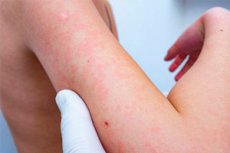
Meskipun pengobatan sering kali membantu pasien pulih atau memperbaiki kondisinya, jutaan orang di seluruh dunia menderita reaksi toksik yang tidak terduga terhadap obat setiap tahunnya. Secara khusus, ruam obat, yang muncul dengan gejala seperti kemerahan, melepuh, dan gatal pada kulit, cukup umum terjadi.
Ruam obat yang parah dapat mengancam jiwa dan memiliki efek jangka panjang. Oleh karena itu, memahami bagaimana dan mengapa ruam obat terjadi merupakan bidang penelitian penting dalam ilmu kedokteran.
Untuk mencapai tujuan ini, penelitian sebelumnya telah mengidentifikasi varian spesifik pada gen tertentu sebagai agen penyebab ledakan obat yang potensial. Para ilmuwan percaya bahwa gen yang mengkode antigen leukosit manusia (HLA), suatu protein yang diekspresikan pada permukaan sel darah putih yang memainkan peran penting dalam sistem kekebalan tubuh, terlibat dalam ruam obat. Namun, teori yang ada saat ini tidak dapat menjelaskan mengapa erupsi obat terkait HLA biasanya muncul di kulit dibandingkan di beberapa organ di seluruh tubuh.
Untuk mengatasi kesenjangan pengetahuan ini, tim peneliti yang terdiri dari anggota fakultas Shigeki Aoki, Kousei Ito, dan Akira Kazaoka dari Sekolah Pascasarjana Ilmu Kedokteran dan Farmasi Universitas Chiba melakukan studi mendalam tentang hubungan antara HLA dan erupsi obat. Hasilnya dipublikasikan di PNAS Nexus.
Para peneliti pertama kali melakukan serangkaian percobaan pada keratinosit tikus, yang merupakan jenis sel utama yang ditemukan di kulit. Keratinosit ini telah dimodifikasi untuk mengekspresikan varian spesifik gen HLA yang disebut HLA-B57:01, yang secara spesifik berikatan dengan obat antivirus abacavir. Mereka kemudian mengkonfirmasi hasil ini pada tikus hasil rekayasa genetika yang mengekspresikan HLA-B57:01 yang dipapar dengan abacavir.
Para peneliti menemukan bahwa keratinosit yang mengekspresikan HLA-B*57:01 dan terpapar dengan abacavir menunjukkan respons stres retikulum endoplasma (ER), seperti pelepasan kalsium segera ke dalam sitosol dan peningkatan ekspresi heat shock protein 70 (HSP70). Mereka juga mengamati peningkatan produksi sitokin dan migrasi sel kekebalan. Paparan abacavir menyebabkan kesalahan pelipatan HLA di UGD sehingga menyebabkan stres ER.
Selanjutnya, para peneliti telah menemukan bahwa tekanan ER dapat dikurangi dengan menggunakan 4-fenilbutirat (4-PB). Dengan menghilangkan stres ini, mereka mampu menekan timbulnya gejala ruam obat yang parah. Pengetahuan baru ini dapat memberikan dasar bagi pilihan pengobatan inovatif untuk ruam akibat obat.
Tetapi bagaimana informasi baru ini berbeda dengan apa yang telah diketahui tentang HLA?
"Molekul HLA adalah komponen integral dari sistem kekebalan tubuh kita, biasanya menghadirkan antigen asing ke sel darah putih, yang menilai antigen ini sebagai antigen sendiri atau bukan. Dalam peran yang sudah mapan ini, HLA biasanya memainkan peran kecil," jelas Dr..Aoki.
"Namun, penelitian kami menyoroti fungsi baru molekul HLA dalam sel kulit. Kami menemukan bahwa genotipe HLA spesifik dalam keratinosit dapat mengenali obat tertentu sebagai benda asing, sehingga menyebabkan respons stres retikulum endoplasma."
Secara keseluruhan, hasil penelitian ini mengungkapkan peran baru protein HLA dalam mendeteksi dan merespons potensi ancaman pada sel kulit. Dengan demikian, fungsinya mungkin lebih dari sekedar presentasi antigen pada sistem kekebalan tubuh. Selain itu, mengingat varian HLA seseorang dapat ditentukan melalui pengujian genetik, penelitian ini dapat membantu mengembangkan tindakan pencegahan dan metode diagnostik terhadap reaksi obat merugikan yang parah.
Menurut Dr. Aoki, hal ini sejalan dengan arah dan tren ilmu kedokteran saat ini. "Dalam 10 tahun, kami memperkirakan akan memasuki era 'keseluruhan genom', ketika pengobatan yang dipersonalisasi berdasarkan genom individu akan menjadi praktik standar," komentarnya.
"Berdasarkan hasil penelitian ini, kami percaya bahwa pemahaman komprehensif tentang mekanisme yang mendasari reaksi obat merugikan yang bergantung pada HLA akan memungkinkan perawatan kesehatan yang aman sekaligus memungkinkan pasien menghindari penderitaan yang tidak perlu akibat efek samping."
Secara keseluruhan, penelitian masa depan dalam bidang ini dapat meminimalkan terjadinya ruam obat dan menyelamatkan orang dari efek samping obat yang berpotensi fatal.
