Publikasi baru
FDA menyetujui terapi baru untuk pasien glioma untuk pertama kalinya dalam beberapa dekade
Terakhir ditinjau: 02.07.2025

Semua konten iLive ditinjau secara medis atau diperiksa fakta untuk memastikan akurasi faktual sebanyak mungkin.
Kami memiliki panduan sumber yang ketat dan hanya menautkan ke situs media terkemuka, lembaga penelitian akademik, dan, jika mungkin, studi yang ditinjau secara medis oleh rekan sejawat. Perhatikan bahwa angka dalam tanda kurung ([1], [2], dll.) Adalah tautan yang dapat diklik untuk studi ini.
Jika Anda merasa salah satu konten kami tidak akurat, ketinggalan zaman, atau dipertanyakan, pilih dan tekan Ctrl + Enter.
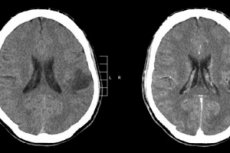
Vorasidenib telah disetujui oleh Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) untuk pasien dengan glioma tingkat 2 dengan mutasi IDH1 atau IDH2.
Berdasarkan data dari uji klinis INDIGO, uji klinis global fase III, double-blind, acak, vorasidenib meningkatkan kelangsungan hidup bebas progresi hingga lebih dari dua kali lipat dan menunda kebutuhan pengobatan dengan radiasi dan kemoterapi pada pasien dengan glioma IDH-mutant grade 2 setelah operasi reseksi tumor. INDIGO adalah uji klinis fase III pertama dari terapi tertarget untuk glioma IDH-mutant.
"Studi INDIGO menunjukkan bahwa inhibitor IDH dapat bekerja pada glioma tingkat rendah dengan mutasi IDH," kata Patrick Wen, MD, direktur Pusat Neuro-Onkologi di Dana-Farber Cancer Institute dan salah satu dari tiga ketua studi tersebut. "Obat terakhir yang disetujui untuk glioma tingkat rendah disetujui pada tahun 1999, jadi ini akan menjadi obat baru pertama dalam waktu yang lama."
Glioma tingkat 2 adalah tumor otak yang tidak dapat disembuhkan. Mutasi IDH ditemukan pada sebagian besar glioma tingkat rendah.
Manfaat utama terapi vorasidenib adalah dapat menunda kebutuhan radiasi dan kemoterapi. Perawatan saat ini melibatkan pembedahan yang diikuti oleh radiasi dan kemoterapi. Radiasi dan kemoterapi merupakan perawatan yang efektif, tetapi setelah bertahun-tahun menjalani perawatan, pasien mulai mengalami tanda-tanda disfungsi kognitif yang biasanya terlihat pada orang yang jauh lebih tua.
"Pasien-pasien ini sering kali masih muda, berusia 30-an atau 40-an. Namun, 10 hingga 20 tahun kemudian, meskipun tumor mereka membaik, mereka sering kali menunjukkan tanda-tanda demensia setelah radiasi dan kemoterapi," kata Wen. "Jika obat ini dapat menunda dimulainya perawatan tersebut, obat ini dapat menunda disfungsi kognitif pada pasien dan mempertahankan kualitas hidup mereka."
Studi INDIGO melibatkan 331 pasien dengan glioma IDH-mutant grade 2 yang menjalani operasi pengangkatan tumor. Pasien yang terdaftar dalam studi ini tidak memerlukan radiasi atau kemoterapi segera dan berada dalam periode tindak lanjut. Selama periode ini, mereka diacak untuk menerima vorasidenib atau plasebo.
Pasien yang mengonsumsi vorasidenib memiliki median kelangsungan hidup bebas progresi sebesar 27,7 bulan, dibandingkan dengan 11,1 bulan untuk pasien yang mengonsumsi plasebo. Waktu untuk perawatan berikutnya bagi pasien yang mengonsumsi plasebo adalah 17,8 bulan.
Pada pasien yang diobati dengan vorasidenib, median belum ditentukan pada saat analisis terakhir, karena hanya 11,3% dari pasien tersebut yang telah beralih ke pengobatan berikutnya sejauh ini. Obat tersebut juga memiliki profil keamanan yang dapat dikelola.
"Studi ini tidak menemukan perbedaan dalam kualitas hidup dibandingkan dengan plasebo," kata Wen. "Tolerabilitas penting karena ini adalah obat yang kami harapkan dapat dikonsumsi orang selama bertahun-tahun."
Persetujuan ini membuka beberapa opsi baru bagi pasien. Misalnya, Van tengah melakukan studi yang mengkaji vorasidenib dalam kombinasi dengan imunoterapi, dan studi yang menggabungkan vorasidenib dengan radiasi dan kemoterapi standar sedang direncanakan.
